特定臨床研究にご協力いただく5歳から12歳の自閉スペクトラム症のお子さんの募集を終了いたします。たくさんのお問い合せ、誠にありがとうございました。
今回の臨床研究の中間報告は、9月17日の第7回腸内フローラ移植臨床研究会の学術大会で発表いたします。誰もが安心して受けられる医療として確立するため、どうか引き続きご理解・ご支援のほどよろしくお願いいたします。

1. はじめに
臨床研究とは、患者さんに参加・ご協力いただき、治療法や診断法の安全性と有効性を調べる研究のことをいいます。現在行われている多くの治療法・診断法も、国内外での臨床研究によって進歩してきました。
本研究は、企業が主体となって行う「治験」とは異なり、研究者(医師)が主体となって行うものです。
本臨床研究は、認定臨床研究審査委員会で承認された後、臨床研究を実施する各医療機関の院長が研究実施を承認し、臨床研究の研究代表医師が厚生労働大臣に実施計画を提出した上で、実施するものです。
2. 自閉スペクトラム症について
自閉スペクトラム症(ASD)とは、対人関係が苦手、こだわりが強い、感覚が過敏などの特徴がある発達障害のひとつです。
ASDは、2013年にアメリカ精神医学会の診断基準DSM-5(精神障害の診断・統計マニュアル第5版)で発表された疾患名です。それ以降、それまで自閉症、広汎性発達障害、アスペルガー(Asperger)症候群など様々な名称で呼ばれていた疾患をまとめてASDと表現されるようになりました。
ASDは、さまざまな要因が複雑に関与して起こる脳機能障害であると云われています。
ASDの発症数は国内外において年々増加しており、大きな社会問題にもなっています。
ASDの原因は、未だ特定されておらず、根本的な治療法も開発されていません。ASDによる症状や困りごとを軽減するための対処法として、「ASDの症状に合わせた環境調整」、また「カウンセリング・心理療法」があります。しかし、このような対処法に即効性はなく、施行できる専門家も少ないのが現状です。
また、薬物療法として、非定型抗精神病薬(例:リスペリドン、アリピプラゾール)、気分安定薬(例:バルプロ酸)、精神刺激薬などがありますが、これらはASDの辺縁症状にのみ有効であり、中核症状に対する有効性は認められていません。
このように、効果発現が早く、効果量の大きい新しい治療法の開発が強く望まれている分野です。
3. 腸内細菌叢移植とは
腸内細菌叢移植(FMT)は、糞便微生物叢移植あるいは腸内フローラ移植とも言われています。腸内の細菌叢を改善する目的で、健常人の糞便から調製した糞便微生物溶液を患者さんの腸内に移植する治療法です。
新規FMT方法(以下NanoGAS‐FMT法)は、従来の方法で一般的に行われている「FMT施行前の抗菌薬投与や腸管洗浄」を必要としません。便の溶解に従来法で使われている生理食塩水の代わりに、シンバイオシス(株)が独自に開発した安定な水素ナノバブル水を使用しており、内視鏡を使わず細いゴム状の管で直腸に注腸する、お子さんの負担が少ない方法です。
また「従来法で用いられている投与量(細菌数)の約1000分の1」の少量の投与量をもって実施する新しい方法として開発しているものです。
図1.NanoGAS‐FMT法と従来のFMT法との違い(概念図)
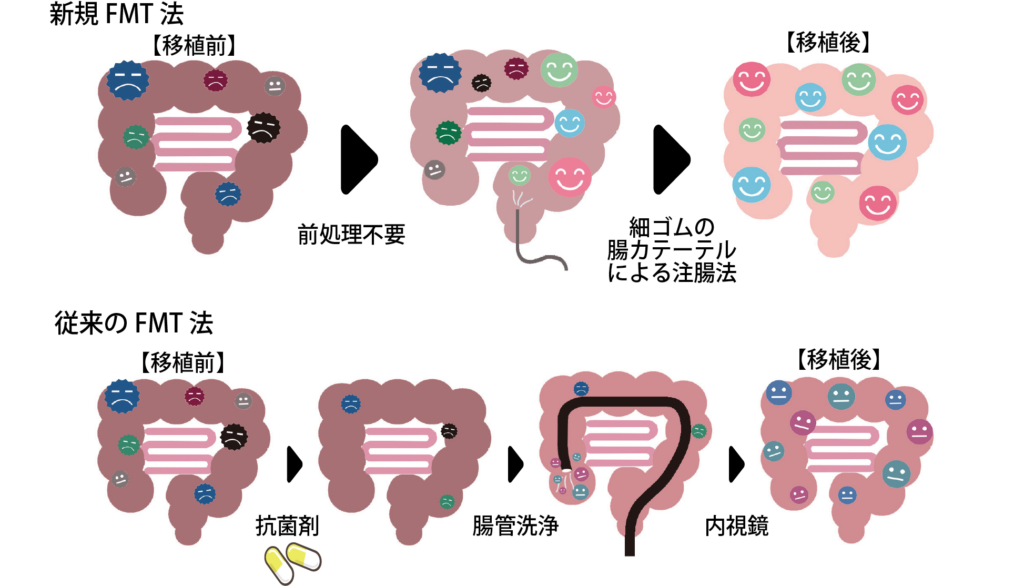
相違点は以下の通りです。
①NanoGAS‐FMT法
* 細くて柔らかいゴム状のチューブを用いて、ASD児の肛門から近い直腸部位に糞便微生物溶液を投与します。3~5分で終了いたします。これで移植は終了いたします。
② 従来のFMT法 (アリゾナ大学の例)
- * 抗菌薬・バンコマイシンを2週間、毎日連続投与。
- * 2週間後、腸管洗浄剤PEGで腸を洗浄。
- * 大量(細菌数としてNanoGAS‐FMT法の場合の1000倍量以上)の糞便微生物溶液を2日間、毎日経口(または直腸)投与。
- * 細菌数として、NanoGAS‐FMT法の初期投与の場合の約10倍量を含むカプセル剤を約60日間、連続投与。
- * 同時に胃酸分泌抑制薬を約60日間、連続投与。
2022年11月、米国・FDA(アメリカ食品医薬品局)は、フェリング社が開発した「糞便微生物製剤・Rebyota 」を再発性クロストリジオイデスディフィシル感染症の治療薬として承認しました。今後の、様々な疾患に対するFMTの臨床研究・治験が加速されるものとして、注目されています。
https://www.ferring.co.jp/category/global-2022/
なお、米国及び中国で行われた「FMTによるASD児の治療」に関する先行研究、また、米国及び中国において、現在進行中の「臨床研究から一歩進んだ治験」においては、下表のとおり、研究対象者の年齢は、それぞれ2歳及び3歳まで引き下げられています。
米国の場合はFDAが承認しているものです。また、最も厳しいとされる、中国の場合もCFDAが認めているものもあります。
表 先行研究及び現在進行中の治験における研究対象者の年齢層
| 実施機関 | ステージ | 研究対象者の年齢層 |
| アリゾナ大 | 先行臨床研究 | 7歳-17歳 |
| 第三軍医大 | 先行臨床研究 | 3歳-17歳 |
| ProgenaBiome | 治験 | 2歳以上 |
| Ventura C.Trials | 治験 | 2歳以上 |
| LA小児病院 | 治験 | 5歳-17歳 |
| アリゾナ大 | 治験 | 5歳-17歳 |
| 武漢大学 | 治験 | 3歳-18歳 |
すでに私たちは、倫理審査委員会で承認を受け、上記の「NanoGAS‐FMT法」を、初めに5歳から12歳のASDのお子さん(14名)の治療に適応しました。
お子さんのご両親からの同意を得て、この自由診療の結果を解析した結果、NanoGAS‐FMT法がお子さんのASD症状を軽減することが分かりました。
図2は、個々の症例に関して、SRS-2による重症度の変化を表したものです。
「NanoGAS‐FMT法」によって、移植後8週において、14名の方々のうち、重度の6名を含めた10名(71%)の方々のASD症状が大きく軽減されました。
図2.「SHIN-1を用いるFMT法」のASDに対する有効性
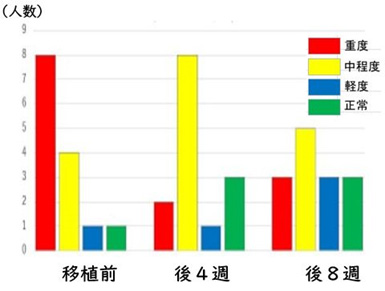
その結果、上記の14症例を用いた治療成績において、1症例において、疲れ・便秘の有害事象が認められたが、それらは軽微で一時的でした。
4. 研究の方法
1)対象となるお子さん
この研究は、ASDと診断されたお子さんのうち、以下の条件を満たす方を対象としています。
なお、担当医師の判断によっては参加できないこともあります。
【参加していただけるお子さんの条件】
・小児神経専門医、精神神経学会認定専門医、児童青年精神医学会認定医、或いは小児精神神経学会認定医のいずれかの専門医・認定医により、ASDの診断をされた5歳から12歳までのお子さん
(要診断証明書*1、性別は不問)
・研究責任医師が、胃腸の症状を除けば、一般的に良好な身体的健康状態であると判断したお子さん
・本研究への参加について、文書、あるいは必要に応じてイラストや口頭で説明することにより同意が得られるお子さん
・本研究への参加について文書による同意が代諾者から得られるお子さん
*1:診断書が未取得の方はこちらのサイトをご確認いただき、診断書の取得をお願いいたします。
日本小児神経学会が認定する小児神経専門医の名簿:
https://www.childneuro.jp/modules/senmoni/
精神神経学会認定専門医の専門医一覧:
https://www.jspn.or.jp/modules/senmoni/
日本児童青年精神医学会の認定医一覧:
https://child-adolesc.jp/nintei/ninteii-ichiran/
小児精神神経学会認定医の認定医一覧:
https://www.jsppn.jp/physician
【参加していただけないお子さんの条件】
・薬物治療施行中である方
・過去3か月以内に抗生物質(局所抗生物質は除く)の投与を受けた方
・過去12ヶ月以内にFMTを実施したことがある方
・ASD様症状を示す単一遺伝子障害(脆弱X症候群、レット症候群、Joubert(ジュベール)症候群など、効果判定に影響を及ぼす可能性がある疾患)である方
・脳神経外科・脳神経内科疾患のある方
・経管栄養を行っている方
・標準体重の65%未満の体重不足/栄養不足である方
・一年以内に手術をしたか、あるいは半年以内に手術を予定している方
・現在、他の臨床試験に参加中である方
・その他の理由で、担当医師によって、参加が適切ではないと判断した方
2)試験デザイン
注腸液の投与の前後の検査値を比較することにより、「NanoGAS‐FMT法」の有効性と安全性を評価いたします。倫理面を考慮し、対象群を設けずに行います。
3)腸内細菌叢移植(FMT法)の手順
(1) ドナーの健康状態、ドナー便の安全性、ドナー便の保管・使用
(ドナー:糞便を提供していただく方)
①ドナーの健康状態
使用する便は、登録されたボランティアのドナーから提供されます。担当の医師は、ドナーに対する、診察・検査(約150項目の問診票及び以下の広範囲におよぶ血液検査)を、2~3か月に一回程度の頻度で行い、それを基にドナーの健康状態をチェックします。
<問診票>
年齢、性別、身長、体重、抗生物質使用歴、自然分娩/母乳育児、既往歴、薬やサプリメントの使用状況、渡航歴、食習慣、睡眠習慣、等
<医師による診察>
*血圧、脈拍、聴診、尿検査
*血液一般検査:
*生化学・免疫検査:
*感染症検査:
*免疫機能検査:
*腫瘍マーカー検査:
②ドナー便の安全性
便検査も耐性菌検査・食中毒検査・免疫学検査、また細菌の遺伝子検査のそれぞれの細項目の検査を行い、安全性を確認します。
*16S rRNA腸内細菌叢の遺伝子解析
*耐性菌検査
*食中毒検査
*免疫学的検査
③ドナー便の保管・使用
安全と判断した便は−80℃で保管されます。上記の2~3か月に一回行う次の検査で、医師によって合格と判断された時点で、凍結した便を使用します。
この原液の調整工程は、シンバイオシス社において、医薬品製造と同様の環境下である治験薬GMPの下で行います。
全てに操作は、汚染の全くない安全キャビネットの中で行われます。
原液を調製する安全キャビネット

(2) 注腸液の調製と投与量
以下の調製操作は、医療機関で行います。
お子さんの中には、注腸液の投与に抵抗を示すお子さんもおられる可能性があることから、最初は、注腸液の濃度を薄くして、徐々に濃度を上げていく投与方式をとることによって、注腸投与に慣れてもらえるようにしました。
(3) 注腸液の投与方法
注腸液を1週間に1回、連続6週間、計6回、注腸投与します。1回あたりの投与時間は3~5分間です。他の検査なども含めて、1回の診療に要する時間は30~45分程度です。
また、注腸時には、細いゴム管(直径6.5mm)を使います。感覚過敏なお子さんにとっては、違和感がある場合もありますが、侵襲性の低い方法です。
投与開始後、30週目の結果をもって、有効性の最終評価を行います。

これまで幼児16名に対して、糞便微生物溶液(SHIN-1)の注腸投与を行ってきました。抵抗度合いを、泣き具合から(図5)、また抵抗することによる液漏れ(図6)から示しました。回を重ねる毎に抵抗が無くなっていく様子がみられます。
図4.注腸時の抵抗度合い(泣き具合)
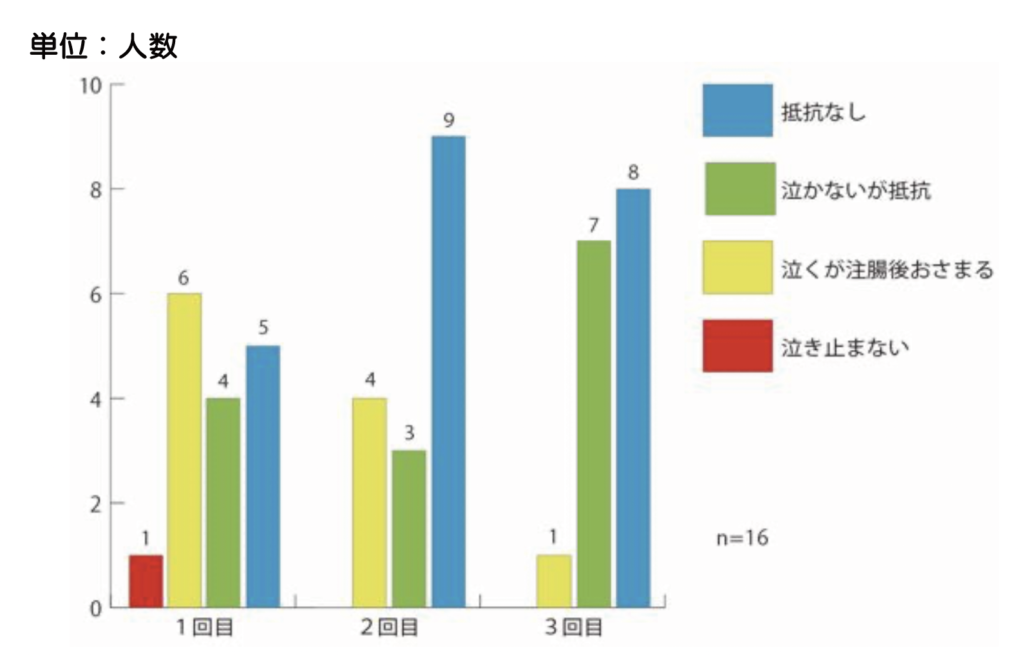
図5.注腸時の抵抗度合い(暴れによる液漏れ)
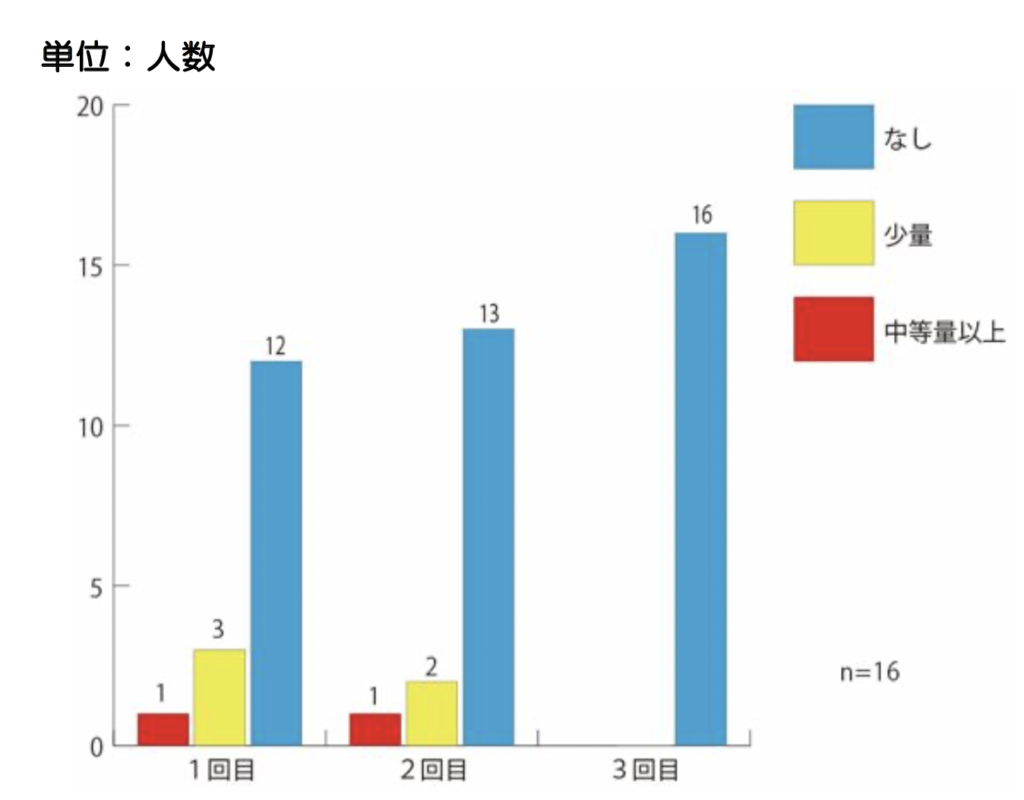
4) 検査について
(1) ご自宅で行っていただく検査
以下の4つの項目で、いずれも質問票にお答えいただく検査です。
・SRS-2(対人応答性尺度)
(マークシート方式)
・PHQ-4(うつ病と不安の4項目の尺度)
・GSRS(消化管症状チェックリスト)
・BSスコア(便の状態変化の記録)
(2) 医療機関で行う検査
・視線計測装置 Gazefinder(ゲイズファインダー)
この機器は、2分程度の動画を見て、どこを見ていたかなど、ものの見方からASDの特性を客観的に評価する一つのツールです。画面を見るだけで検査ができますので、お子さんにとって負担が少ない検査です。

(3) ご自宅で採便し、郵送していただく検査
・16S rRNA遺伝子解析(糞便遺伝子検査)
・・・糞便中の細菌分布を調べる細菌遺伝子検査です
・保存用の便
(4) オンラインダイアリー
・検査には該当しませんが、オンラインダイアリーにて、日々の行動の変化などのご入力をお願いいたします。(パソコン、スマートフォンで入力可能です)
・起きた時間、寝た時間や、食事の記録、排便記録、気分などを入力していただくものです。
・かんしゃくやこだわりなど、行動の変化などを自由記入欄に入力していただきます。
5)スケジュール表
各種検査項目の実施時期をまとめました。
ご不明な点がございましたら、臨床研究事務局までご連絡をください。
表3.スケジュール表
-883x1024.jpg)
6)研究終了後における医療の提供
この研究の治療が終了した後も、必要に応じてFMTを施行することができます。その場合は、この方法が、将来保険適用されるまでは、自由診療となります。
5. 実施予定期間と目標症例数
1)研究対象者の募集期間
jRCT公開日から目標症例数(30名)に達するまで。
2) 臨床研究の観察期間
初回FMT施行から30週まで。
6. 予想されるご負担
(1) 交通費と時間の消費
通常診療に比べて来院頻度が増加するため、通院時間や交通費が増える可能性があります。(臨床研究開始前の自由診療による診察と、移植のための来院6回、あと観察のための来院3回の通院時間と交通費)また、ご自宅で行っていただく、SRS-2、GSRS及びPHQ-4の検査のための質問紙の記載に30分程度、またダイアリーの記載に10分程度の時間がかかります。移植前、移植開始8週後と30週後に16S rRNA遺伝子検査を行います。ご自宅でお子さんの便を専用のキット採取し、郵送で送っていただく検査ですが、便の採取や郵送に手間と時間がかかります。
(2) 臨床研究開始前の自費診療の内容とかかる費用
臨床研究組み入れ前に要する費用(税別)
| 診察費用(臨床所見(診察)、身長、体重、 血圧、体温、聴診、脈拍、SpO2) | 1万円程度/回 ※時間による変動あり |
※その他、必要に応じて各種検査(尿検査、血液検査等)が追加される場合があります。
※移植のための診察・移植処置費6回分、後観察のための診察3回分に関して費用は発生しません。
(3) 臨床研究参加中の医薬品の服用
医薬品によっては、研究参加中の服用を中止するようお願いすることがあります。
(4) 有害事象
FMTは有害事象の少ない方法として期待されています。注腸液の投与による、14名のうち1名のお子さんに、疲れ・便秘の有害事象は認められましたが、それらは軽微で一時的なものでした。しかし、症例数が増えた場合、有害事象の増加の可能性は否定できません。
2022年4月以降、自由診療の下で実施した、ASD以外の疾患(約50症例)に対するSHIN-1含有注腸液の投与においては、いくつかの症例において、腹痛、便秘、下痢、発熱、等の有害事象が観察されましたが、いずれの事象も軽度で一時的なものでした。
臨床研究中及びその後の診察でも、安全性の管理に努め、重篤な有害事象(副作用など好ましくないすべての事象で、注腸投与との因果関係は問わない)が起こった際には、安全確保を第一優先として、迅速かつ適切な処置を行うことにより、お子さんの安全確保に全力を尽くします。
なお、副作用には個人差があり、必ずおこるというわけではありません。どんな薬でも副作用がおこる可能性はありますので、いつもと違う症状があれば担当医師や末尾のお問い合わせ先・相談窓口までご連絡ください。
7. 本臨床研究への参加について
本研究に参加するかどうかは、お子さんとあなたの自由な意思で決めてください。参加を辞退することもできます。どのような決定をされたとしても、お子さんとあなたの不利益になることはありません。説明文書をよく読んでいただき、参加をご検討の方は、臨床研究事務局にお問い合わせください。
ご家族と相談するなど十分に考えたうえで、研究責任医師が在籍する医療機関(6施設)を受診し、お子さんとあなた自身の自由な意思で決めてください。
ご協力いただける場合は、同意書へご署名をお願いいたします。
8. 同意撤回について
本研究への参加に同意した後にいつでも同意を撤回することができ、たとえお断りになっても今後の治療において不利益を受けることはありません。同意の撤回を希望される場合は、遠慮なく担当医師にお伝えください。
9. 研究に関する情報公開の方法
本研究の目的や方法などの概要は、研究の実施に先立って厚生労働省が整備するデータベース( jRCT: Japan Registry of Clinical Trials, URL: https://jrct.niph.go.jp/ )へ登録し、公開されます。
研究の進捗状況、結果等についてもご覧いただけます。なお、公開の際、個人情報は伏せられ、個人が特定できないようになっています。
10. 費用について
1)注腸液は、シンバイオシス(株)から無償提供されます。そのため、FMTを受けるお子さんの代諾者の金銭的負担が増えることはありません。
2)本研究参加が確定する前の診察時は自費診療として1~2万円程度の費用が発生する場合があります。(診察料等)
3)あなたに対して謝金等の支払いは行われません。
4)交通費や遠方よりお越しで宿泊を要した場合の費用は、自己負担となりますので予めご了承ください。
11. 健康被害が生じた場合の補償について
本研究は細心の注意を用いて行いますが、万一、本研究に関連してお子さんに健康被害が発生した場合には、当院において速やかに最善の治療を行います。 何らかの健康被害が発生した場合の補償は、賠償責任保険(臨床研究等保険)の契約条件に従って補償を行います。
12. 実施医療機関の名称並びに担当医師の氏名・職名・連絡先
【研究代表医師】(研究全体を統括する研究者)
医療法人仁善会 田中クリニック 理事長 田中 善
| 医療法人仁善会 田中クリニック | 大阪府生野区生野西2-3-8 電気館ビル1階 06-6711-3770 | 田中 善 | 理事長 | https://www.tanaka-cl.com/fmt.html |
| ルークス芦屋クリニック | 兵庫県芦屋市大原町8‐2 0797-23-6033 | 城谷 昌彦 | 院長 | https://www.lukesashiya.com/feature/flora.html |
| 医療法人喜和会 喜多村クリニック | 福岡県大野城市錦町4-3-8 092-581-6640 | 喜多村 邦弘 | 院長 | http://www.kitamura.or.jp/contents_fmt.html |
| 医療法人悠亜会 かわい内科クリニック | 大阪市城東区東中浜3-7-14 06-6962-3133 | 川井 勇一 | 理事長 | https://www.kawai-medical.com/diagnosis02/ |
| 医療法人ふたまた会 ナチュラルアートクリニック | 東京都千代田区六番町6‐5 アンドロイドビル2F 03-6256-8448 | 御川 安仁 | 院長 | https://naturalartclinic.com/alternative-therapy/1549 |
| 医療法人 はるなクリニック | 大阪府大阪市淀川区西三国 1丁目3‐13‐202 06-4807-5130 | 春名 令子 | 副院長 | https://www.haruna-clinic.com/541-2 |
13. 臨床研究等提出・公開システムで確認する
jRCT(臨床研究等提出・公開システム)にて公開しています。
https://jrct.niph.go.jp/latest-detail/jRCTs031230041
関連記事
2024年9月22日開催!第8回学術大会
特定臨床研究の結果報告を発表いたします。
詳細は以下よりご覧ください。















